2025年成考高起点每日一练《理化综合》3月10日专为备考2025年理化综合考生准备,帮助考生通过每日坚持练习,逐步提升考试成绩。
单选题
1、0.2mol有机物燃烧时从空气中吸收0.3molO2,产生4.48L(标准状况)CO2和7.2gH2O,则该有机物的分子式为()。
- A:CH4
- B:CH2O
- C:CH3OH
- D:CH2O2
答 案:C
2、把小球以初速度ν0=30m/s竖直上抛,忽略空气阻力,4s时小球运动的位移和路程分别是()。(取g=10m/s2)
- A:4045m
- B:40m,50m
- C:45m,40m
- D:50m,40m
答 案:B
解 析:本题的考点是竖直上抛运动,用竖直上抛运动的有关公式解题。解本题的关键是区别位移和路程的不同概念。位移是矢量,既有大小又有方向;路程只有大小。位移的大小是物体运动的起始点到终止点之间的直线距离,而路程是物体运动中所经过的轨道的长度。 竖直上抛运动可以分成上升和下落两个过程,运动的转折点是最高点。在上升阶段中,位移 的大小等于路程,在下落阶段中两者并不相等。
根据竖直上抛运动的公式,物体的上升时间为 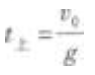 代入题给数值得
代入题给数值得 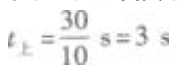 由此可知4s时物体处于下落过程,位移的大小与路程不相等。
由此可知4s时物体处于下落过程,位移的大小与路程不相等。
由竖直上抛运动的位移公式得 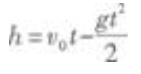 代入已知数值得
代入已知数值得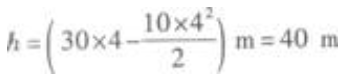 由此可以排除C、D.
由此可以排除C、D.
物体的路程为上升的路程和下落时的路程之和,即
s=s上+s下
显然s上=H,物体下落时做自由落体运动,运动的时间为
t下=t-t上=4s-3s=1s
按照自由落体运动的公式知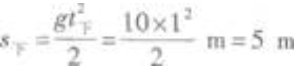 竖直上抛运动上升的高度为
竖直上抛运动上升的高度为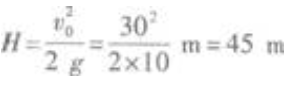 因此物体在4s时运动的路程为
因此物体在4s时运动的路程为
s=H+s下=45m+5m=50m
故选B.
显然,在计算s下时可以由H和h直接计算:
s下=H-h
故有
s=H+(H-h)=2H-h
=2×45m-40m=50m
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: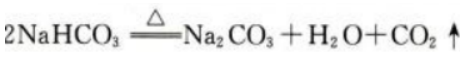 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
2、一绝缘细绳上端固定,下端连接在一质量m=0.08kg、长度l=0.4m的均匀金属棒中心,整个装置处在一匀强磁场中,磁场的磁感应强度大小B=0.5T,方向竖直向上,如图所示。现使一电流流过金属棒,已知电流大小I=3A,方向垂直于纸面向里,重力加速度大小g取10m/s2。求
(1)金属棒所受安培力的大小和方向。
(2)平衡后细绳中张力的大小及细绳与竖直方向夹角的正切值。
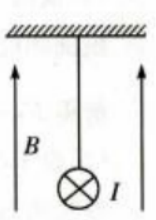
答 案:.(1)金属棒所受安培力为F=BIL=0.6N,根据左手定则知,方向水平向右。 (2)金属棒所受重力为G=mg=0.8N平衡后,安培力与重力的合力与绳中张力等大反向,设细绳与竖直方向的夹角为θ,则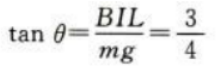 绳中张力大小为
绳中张力大小为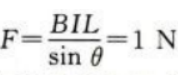
填空题
1、从距地面高为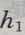 =1.25m处竖直向下抛出皮球,碰地后皮球跳起的高度
=1.25m处竖直向下抛出皮球,碰地后皮球跳起的高度 =2.5 m,不计空气阻力,设球碰撞地面时无机械能损失(g取10m/
=2.5 m,不计空气阻力,设球碰撞地面时无机械能损失(g取10m/ ),则皮球下抛时的初速度大小是()
),则皮球下抛时的初速度大小是()
答 案:5
解 析:皮球碰撞地面时的速度为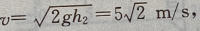 皮球下抛时的初速度为
皮球下抛时的初速度为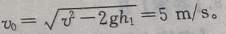
2、如图1-10所示,细线的上端固定于O点,下端系一个小球P,线长l=1.56m,已知小球在水平面内做以O'为圆心的匀速圆周运动,悬线与竖直方向的夹角θ=45°。求
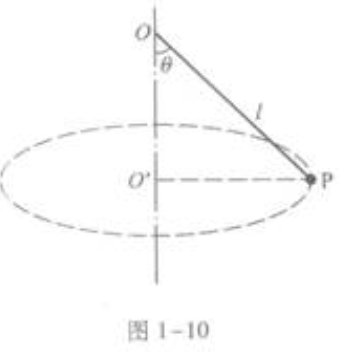
答 案:5.0rad/s
解 析:本题是匀速圆周运动的试题,它的考点有牛顿第二定律和向心力。 以小球为研究对象,小球受两个作用力,细线的拉力FT和重力G。FT沿细线向上,G竖直向下,图1-17是它的受力图。  小球在水平面内做匀速圆周运动,它所受的合外力是匀速圆周运动的向心力。因此,重力G和拉力FT的合力就是向心力F。 取平面直角坐标如图所示。
小球在水平面内做匀速圆周运动,它所受的合外力是匀速圆周运动的向心力。因此,重力G和拉力FT的合力就是向心力F。 取平面直角坐标如图所示。
FT的分量为
FTX=FTsinθ
FTY=FTcosθ
G的分量为
Gx=0
Gy=-mg
水平方向的牛顿方程为
FTx=FTsinθ=F=ma①
竖直方向的牛顿方程为
FTy+Gy=FTcosθ-mg=0
即FTy=FTcosθ=mg②
由式①、②解得
F=mgtanθ=mA.
把向心加速度  代入上式得
代入上式得
F=mRω2=mgtanθ
因此角速度为  圆周运动半径R与线长l的关系是
圆周运动半径R与线长l的关系是
R=lsinθ
代入上式解得  代入题给数值,算得
代入题给数值,算得 
简答题
1、明矾水溶液呈酸性的离子方程式是______,出现浑浊时,消除的方法是______;纯碱与水作用的离子方程式是______,若要增强其洗涤力应______。
答 案:
2、市售锌粉中含有氧化锌等杂质。用3g这种锌粉跟足量的盐酸完全反应,可收集到896mLH2(标准状况),计算这种锌粉中锌的质量分数。
答 案:解:设参加反应的锌的质量为m,则根据化学方程式得: 锌粉中锌的质量分数是ω=
锌粉中锌的质量分数是ω=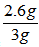 ×100%=86.7% 答:这种锌粉中锌的质量分数是86.7%。
×100%=86.7% 答:这种锌粉中锌的质量分数是86.7%。
精彩评论